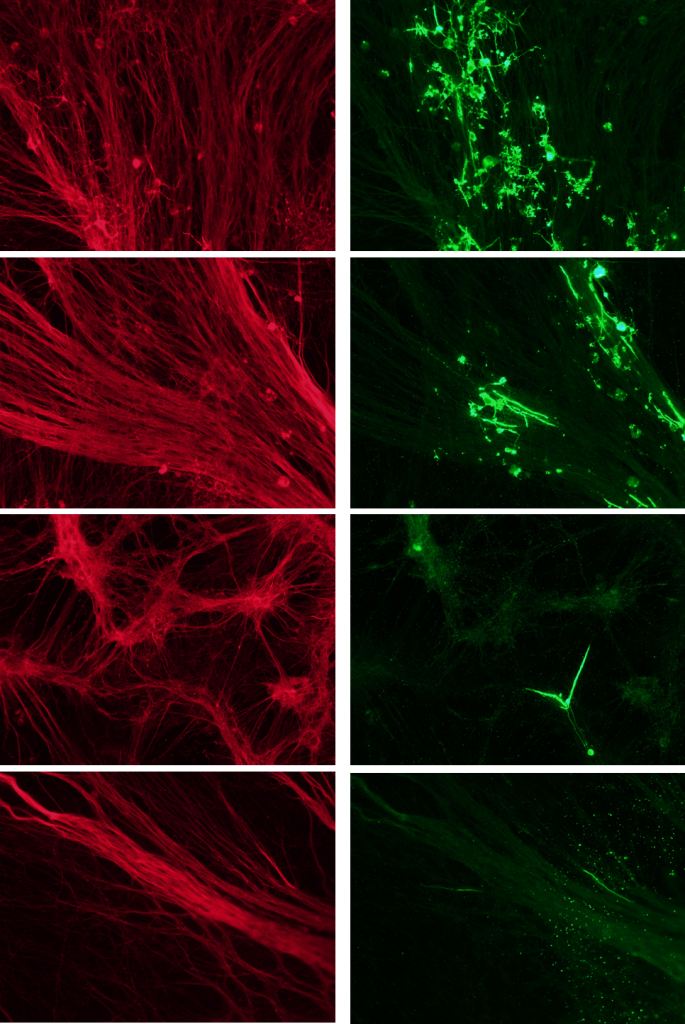
Cojo cubres de todas las condiciones para ir viendo cómo va la diferenciación.
Protocolo:
- Fijar 20 min con PFA 4%
- 1 lavado con PBS1x
- Bloquear con Goat serum 5% y 0’5% tritón (en PBS): 1h a RT (no me ha dado tiempo de bloquear y he hecho un bloqueo/tritón 5 min, y he puesto primero el NFh y después el MBP)
- Incubar con anticuerpos primarios diluídos en Goat serum 5% y 0’5% tritón (en PBS):
- MBP y NFh
- anti-Neurofilament H, AB5539 (Merck) Dil. 1/500 (chicken) : 1h RT
- anti-Myelin basic protein SMI99, 808401 (Biolegend). Dil. 1/100 (mouse) : (1h RT)
- MBP y NFh
- 3 lavados con PBS1x
- Incubar 1h con Ac. secundarios diluídos en Goat serum 5% y 0’5% tritón (todos a 1/500)
- MBP y NFh: GAM488 + GAC594
- 3 lavados con PBS1x
- Montar con Fluoromount
Resultado:
- Explante DRG 01/06/23: marca todas las cels de Schwann… no se ve la mielina como siempre.
- Explante médula 01/06/23: hay mielina
- Médula disgregada 20/07/23 (tratada como co-cultivos): hay un poco de mielina
- Explante DRG coating habitual 20/07/23 (Poly-D/laminina): hay un poco de mielina
- Explante DRG matrigel 20/07/23: no hay mielina
- DRG cels disgregadas matrigel 20/07/23: no se ve bien porque hay demasiadas capas de células!!! No hago foto